

李峻柏课题组在CO2还原驱动ATP仿生合成方面取得新进展
在众多仿生功能中,模拟光合作用或呼吸作用的能量转换机制,是为人工细胞和微纳米机器人提供能量的关键。构建具有类似光合作用或呼吸作用功能的微反应器,不仅有助于更深入地理解生物能量代谢的内在机制,更能推动其在人工生命体系中的应用与集成。
在国家自然科学基金委、科技部及中国科学院的支持下,化学所胶体、界面与化学热力学实验室李峻柏课题组在模拟叶绿体的光合作用和线粒体的呼吸作用方面开展了大量研究,在体外通过多条途径实现了生物能量(ATP)合成(Angew. Chem. Int. Ed. 2025,64,e202417474;Angew. Chem. Int. Ed.2024,63,e202319116; J. Am. Chem. Soc.2023,145,20907−20912;Angew. Chem. Int. Ed.2022,61,e202116220;Angew. Chem. Int. Ed.2021,60,7695-7698)。
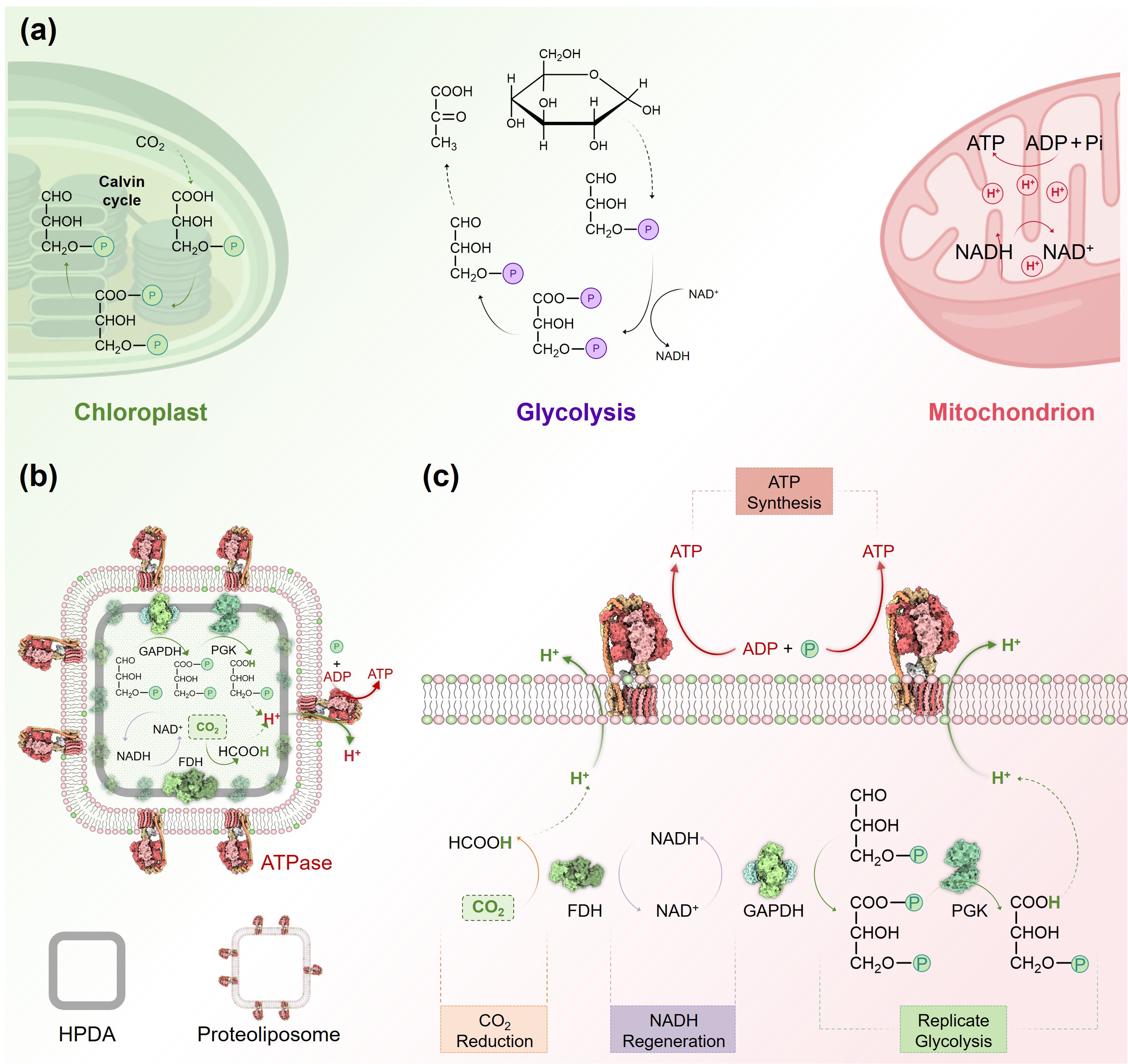
细胞质中的糖酵解过程与叶绿体中的卡尔文循环共享一个关键的级联反应:3-磷酸甘油醛与3-磷酸甘油酸的转化。该反应在糖酵解中表现为从醛到酸的氧化过程,而在卡尔文循环中则恰好相反,为从酸到醛的还原过程。这种精妙的逆向对应,揭示了生物能量代谢更深层次的调控逻辑。受此启发,李峻柏团队设计了一种超分子微反应器(图1)。在该反应器中,甲酸脱氢酶(FDH)催化CO2还原为甲酸,此过程会消耗还原型辅酶Ⅰ(NADH)并产生质子,从而驱动ATP合酶旋转催化合成ATP;而由三磷酸甘油酸脱氢酶(GAPDH)和磷酸甘油酸激酶(PGK)组成的级联催化反应,不仅能将NAD+还原为NADH,实现NADH的循环再生,同时还产生额外的质子进一步促进ATP的合成。本研究通过分子组装技术,在单一微反应器内首次实现了CO2还原、NADH再生和ATP合成的协同耦合,为开发低成本、高效的生物能量转换体系提供了新思路,对拓展生物马达应用具有重要意义。
相关成果近期发表于Angew. Chem. Int. Ed. 2025,64,e202509835,并被选为Frontispiece。论文第一作者是博士后许阳,通讯作者为李峻柏研究员、贾怡副研究员和西安石油大学李红教授。
胶体、界面与化学热力学实验室
2025年12月24日
附件下载: