

化学所在生物分子马达组装体性能调控方面取得新进展
以活性生物大分子为构筑基元,利用分子组装策略设计与构建仿生体系,模拟或调控生命体基本单元的结构和功能,已成为化学与生命科学交叉的前沿和热点。生命体活动所必需的能量来源是三磷酸腺苷(ATP),一般情况下由旋转生物分子马达蛋白ATP合酶在跨膜质子梯度势的推动下合成。
在国家自然科学基金委、科技部和中国科学院的支持下,化学所胶体、界面与化学热力学院重点实验室李峻柏研究员课题组长期致力于生物分子马达ATP合酶的分子组装与应用研究,并取得了系列进展。该研究团队将ATP合酶与光系统II、人工光酸分子或量子点进行共组装,实现了对自然界叶绿体结构的有效模拟和功能的大幅度提升(ACS Nano 2016, 10, 556; ACS Nano 2017, 11, 10175; ACS Nano 2018, 12, 1455; Adv. Funct. Mater. 2018, 28, 1706557; Angew. Chem. Int. Ed. 2017, 56, 12903; Angew. Chem. Int. Ed. 2018, 57, 6532; Angew. Chem. Int. Ed. 2019, 58, 796)。
最近,他们将含有生物分子马达ATP合酶的脂质体铺展在溅射有裸金纳米颗粒的玻璃表面,构筑了一种简易而有效的薄膜型微反应器。研究表明,硫醇分子的引入导致硫醇-金表面自组装单层膜(SAM)的形成,同时产生跨膜质子梯度,进而驱动ATP合酶催化合成ATP。硫醇的种类决定体系中质子梯度形成的动力学,进而调控ATP的合成速率。上述组装的生物分子马达体系将合成的有机小分子转化为生命能量分子ATP,为进一步大面积能量采集及构建ATP驱动的生物分子器件奠定了重要基础。相关研究成果发表在近期的Angew. Chem. Int. Ed. 2019, 58, 1110.
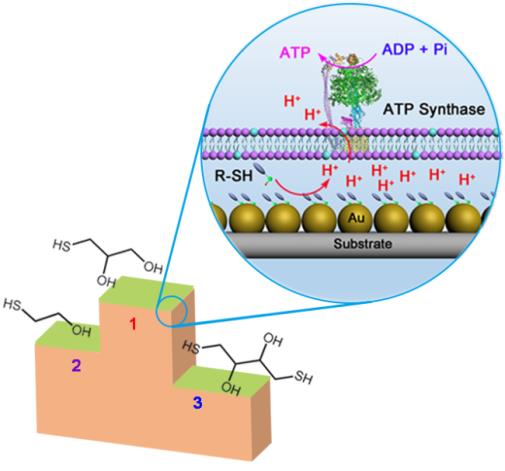
自组装单层技术用于调控生物能量分子的合成
胶体、界面与化学热力学实验室
2019年3月12日
附件下载: