

肖海华课题组在DNA四面体递送高效铂类药物激活STING通路方面取得重要进展
近年来,DNA纳米结构在检测、生物成像、药物靶向递送等生物医学领域内展现出广阔的应用前景。因其高稳定性、良好的生物相容性和易于化学修饰等特点,DNA四面体(TDN)已广泛地用于递送化疗药物、核酸药物并负载荧光探针,实现了肿瘤治疗的诊疗一体化等,受到国内外学者的高度关注。然而,迄今为止,TDN潜在的肿瘤免疫激活效应尚未被挖掘。
在国家自然科学基金委、科技部等项目的支持下,化学研究所高分子物理与化学实验室肖海华课题组围绕生物医用材料和生物安全材料的研究主题,开展了“靶向肿瘤进化的创新纳米药物”和“纳米药物的多组学研究”方向的研究,并在铂类药物载体设计、递送、协同增敏、示踪成像等方面取得了系列研究进展(Nat. Biomed. Eng. 2021, 5, 1048;Adv. Mater. 2022, 34, 2203820;Adv. Mater. 2022, 34, 2105976;Adv. Mater. 2021, 33, 2100599;Angew. Chem. Int. Ed. 2022, 61, e202201486;Angew. Chem. Int. Ed. 2022, 61, e202203546)。
最近,该课题组设计了一种由1条干扰素刺激DNA链(ISD链)和3条特定序列的单链DNA通过碱基互补配对形成的DNA四面体(TDNISDs)。与含ISD序列的二聚体和无ISD序列的TDN相比,TDNISDs可通过其物理拓扑结构和ISD序列来双重激活STING通路,选择性地激活抗原呈递细胞,促进肿瘤抗原特异性T细胞和自然杀伤(NK)细胞浸润肿瘤,展现出更强的免疫激活效应。此外,研究人员还可通过调节ISD链长度,获得含有不同长度ISD序列的TDNs(42bp-TDNISD、64bp-TDNISD和84bp-TDNISD)。通过进一步筛选,研究人员发现84bp-TDNISD具有较佳的免疫激活效果。此外,为进一步提高治疗效果,可向84bp-TDNISD中引入高效铂类DNA嵌入剂 56MESS,最终获得了DNA四面体的纳米药物(84bp-TDNISD/56MESS)。一方面,84bp-TDNISD/56MESS可在胞内快速释放56MESS,后者可在快速杀死癌细胞的同时,激活cGAS-STING通路;另一方面,84bp-TDNISD本身便可有效激活cGAS-STING通路。总之,84bp-TDNISD/56MESS不仅可递送56MESS进行化疗,还可激活cGAS-STING通路,诱导小鼠体内产生抗肿瘤免疫反应,抑制乳腺癌生长,防止发生转移和复发。相关研究成果近期发表在Adv. Mater.2022, DOI: 10.1002/adma.202210267上,硕士生张凌谱为本论文第一作者,肖海华研究员为通讯作者。
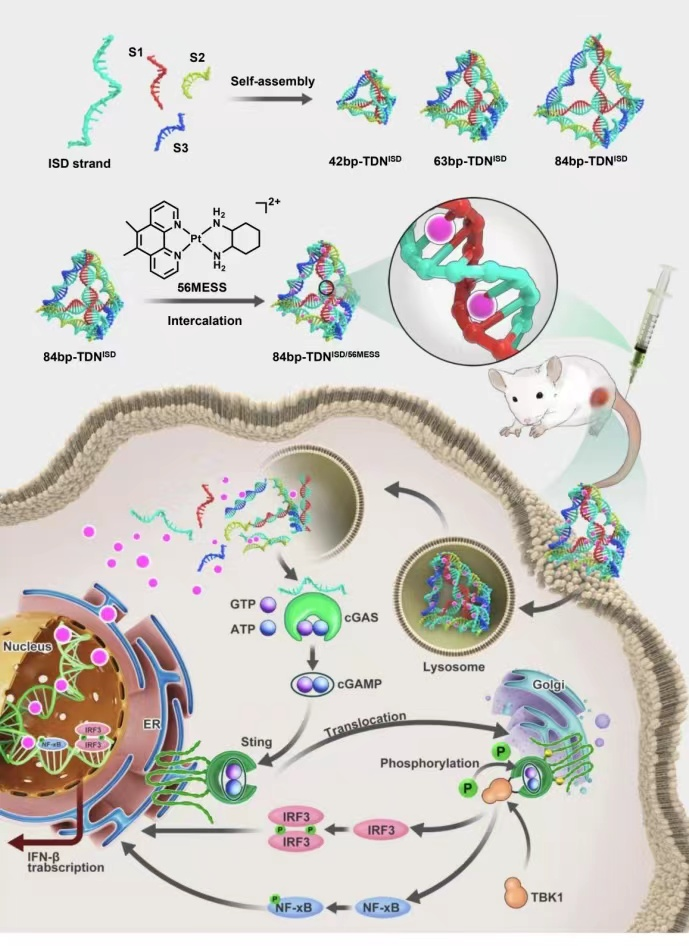
图. 84bp-TDNISD/56MESS通过激活cGAS-STING通路实现高效化疗和免疫治疗
高分子物理与化学实验室
2022年12月19日
附件下载: