

王星等在可控双交联高强水凝胶领域取得新进展
水凝胶作为具有三维交联网络结构的新型高分子软材料,在生物医用、传感器和电学器件等诸多领域应用广泛。然而,目前水凝胶材料仍面临机械性能较差,结构和性能调控手段复杂等问题,不能有效满足复杂器件和生物医学等领域中的功能需求。双网络水凝胶由于其网络结构的选择灵活性和显著的增韧效果在构建高强韧功能化水凝胶的研究进展中备受关注,可逆物理交联网络的引入更是赋予了凝胶更丰富的特性,比如自修复性、刺激响应性、可加工性以及可循环使用等。这种物理交联网络的构建能够精确有效地调控凝胶的结构和性能,促进水凝胶材料在组织工程和再生医学中的广泛应用。
在国家自然科学基金委、科技部和中科院青年创新促进会项目的支持下,化学所高分子物理与化学实验室王星等受双网络水凝胶启发,近年来发现了盐溶液浸泡法诱导壳聚糖形成可逆物理交联网络的策略,建立了简单、便捷、普适制备高强高韧双网络水凝胶的技术,有效地克服了传统水凝胶力学强度低、抗疲劳性差、吸水溶胀后强度劣化以及力学性能调控繁琐的难题(Adv. Mater. 2018, 30, 1707071;Sci. China Chem. 2020, 63, 1793;Chem. Eng. J. 2021, 403, 126431;Carbohyd. Polym. 2022, 276, 118753),进而发展出具有优异生物相容和可降解的壳聚糖基水凝胶,构建了组织工程水凝胶仿生支架,在骨、关节软骨损伤的修复与再生方面取得了实际应用,实现了干细胞定向诱导分化和骨、关节软骨的缺损修复(Adv. Sci. 2022, 9, 2203734;Adv. Sci. 2022, 9, 2105571);再利用稳定、持续、低剂量的药物缓释技术调控骨缺损区域免疫微环境,实现了大面积口腔颅颌面骨缺损的修复与再生(Bioact. Mater. 2022, 11, 130;Bioact. Mater. 2022, 16, 47;Bioact. Mater. 2022, 7, 453;Bioact. Mater. 2023, 20, 194),这些研究工作为组织工程水凝胶支架的生长进程调控和功能重建奠定了扎实的基础。
最近,王星等利用光引发聚合制备壳聚糖/聚N-丙烯酰基甘氨酸(CS/PACG)复合水凝胶,通过一步浸泡处理实现了凝胶力学性能和溶胀性能的同步提高。在浸泡过程中,短链壳聚糖在一价/多价阴离子诱导下形成壳聚糖链缠结/离子交联物理网络,CS/PACG复合水凝胶转化为双网络水凝胶。低价态金属离子介入性地破坏聚N-丙烯酰基甘氨酸链间氢键,进一步与PACG聚合物链中羧基形成离子络合,使凝胶的力学性能显著提高。凝胶表现出超高溶胀性,溶胀1天后体积可达到初始状态的40500倍;此外,高价态金属离子由于可以与羧基形成更强的三齿螯合结构,因此复合水凝胶经过Fe3+和Al3+无机盐溶液浸泡可制备得到机械性能可调的抗溶胀梯度CS/PACG双网络水凝胶。羧基与三价金属离子络合在凝胶表面附近形成疏水致密层,通过改变金属离子种类可以调节致密层的特性,表现出优异的抗溶胀性,溶胀1个月体积未有明显变化,力学性能出现增强。由于不同金属离子与羧基之间金属配位络合能力存在差异,因此简单地更换盐溶液的种类和浸泡顺序就可以实现CS/PACG水凝胶从超溶胀状态到抗溶胀状态的可逆转变,实现凝胶结构和性能的灵活调控,有望在生物医学和组织工程领域中实现更广泛的应用。相关研究成果发表在Adv. Sci.2023, 10, 2206242,论文第一作者为窦雪宇博士,通讯作者为化学所王星副研究员和南方科技大学吴德成教授。
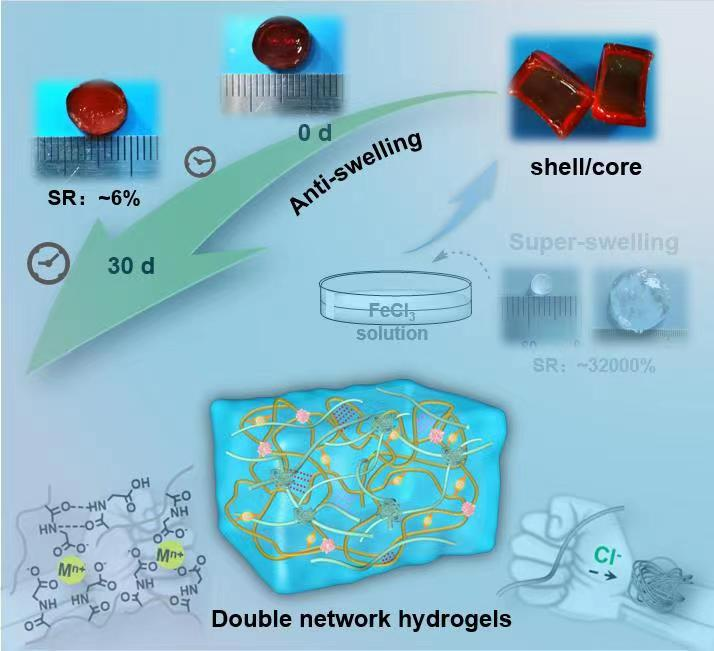
盐溶液浸泡策略制备具有坚硬“盔甲”的抗溶胀水凝胶
高分子物理与化学实验室
2023年5月4日
附件下载: